Lista av föremål
»
Aktinium
»
Antimon
»
Argon
»
Arsenik
»
Barium
»
Bohrium
»
Bor
»
Brom
»
Cerium
»
Cesium
»
Curium
»
Dubnium
»
Erbium
»
Europium
»
Fermium
»
Fluor
»
Fosfor
»
Francium
»
Gallium
»
Guld
»
Hafnium
»
Helium
»
Holmium
»
Indium
»
Iridium
»
Järn
»
Jod
»
Kadmium
»
Kalcium
»
Kalium
»
Kalium
»
Kisel
»
Klor
»
Kobolt
»
Kol
»
Koppar
»
Krom
»
Krypton
»
Kväve
»
Lantan
»
Leda
»
Litium
»
Lutecium
»
Mangan
»
Molybden
»
Natrium
»
Neodym
»
Neon
»
Nickel
»
Nihonium
»
Niob
»
Nobelium
»
Osmium
»
Pengar
»
Platina
»
Polonium
»
Radium
»
Radon
»
Renium
»
Rodium
»
Rubidium
»
Rutenium
»
Samarium
»
Selen
»
Skandium
»
Svavel
»
Syre
»
Tallium
»
Tantal
»
Tellur
»
Tenn
»
Tennesse
»
Terbium
»
Thorium
»
Thulium
»
Titan
»
Uran
»
Vanadin
»
Väte
»
Vismut
»
Volfram
»
Xenon
»
Yttrium
»
Zink
Ar - Argon - INGEN ÄDELGASMETALL
Argon är ett kemiskt element i familjen av ädelgaser, symbol Ar och atomnummer 18. Det produceras genom fraktionerad separation av gaser som finns i luften, främst av syre och kväve. Det är luktfritt, färglöst och inert.
argon är en inert gas i gasform, som bildar åttaatomsmolekyler (argonatomer – Ar8). Dess molära massa är 39,948 g/mol. Dess egenskaper gör den mycket stabil i aseptiska miljöer. Det är den tredje vanligaste ädelgasen i atmosfären och utgör 0,94 % av luften. Dess koktemperatur och ångtryck mättas vid –186°C respektive 0,52 MPa.
argon är en dålig termisk och elektrisk ledare och används därför för lödning och fyllning av elektroniska produkter och för att fylla lysrör. Den används också som skyddsgas, eftersom den är obrännbar och inte kommer att reagera med andra molekyler.
argon används i många applikationer, inklusive metallurgi, för att fylla eld, för tillverkning av kemikalier och isolering, för att fylla lysrör och för att inerta trycksatta kärl och kapslingar där höga temperaturer används. argon används också i gaskromatografianalys för att separera blandningar och mäta koncentrationen av enskilda gaser. Slutligen används argon för tillverkning av läkemedel, till exempel det smärtstillande medlet lidokain.
argon är en inert gas i gasform, som bildar åttaatomsmolekyler (argonatomer – Ar8). Dess molära massa är 39,948 g/mol. Dess egenskaper gör den mycket stabil i aseptiska miljöer. Det är den tredje vanligaste ädelgasen i atmosfären och utgör 0,94 % av luften. Dess koktemperatur och ångtryck mättas vid –186°C respektive 0,52 MPa.
argon är en dålig termisk och elektrisk ledare och används därför för lödning och fyllning av elektroniska produkter och för att fylla lysrör. Den används också som skyddsgas, eftersom den är obrännbar och inte kommer att reagera med andra molekyler.
argon används i många applikationer, inklusive metallurgi, för att fylla eld, för tillverkning av kemikalier och isolering, för att fylla lysrör och för att inerta trycksatta kärl och kapslingar där höga temperaturer används. argon används också i gaskromatografianalys för att separera blandningar och mäta koncentrationen av enskilda gaser. Slutligen används argon för tillverkning av läkemedel, till exempel det smärtstillande medlet lidokain.
Syntetisk
Radioaktiv
Flytande
Gasformig
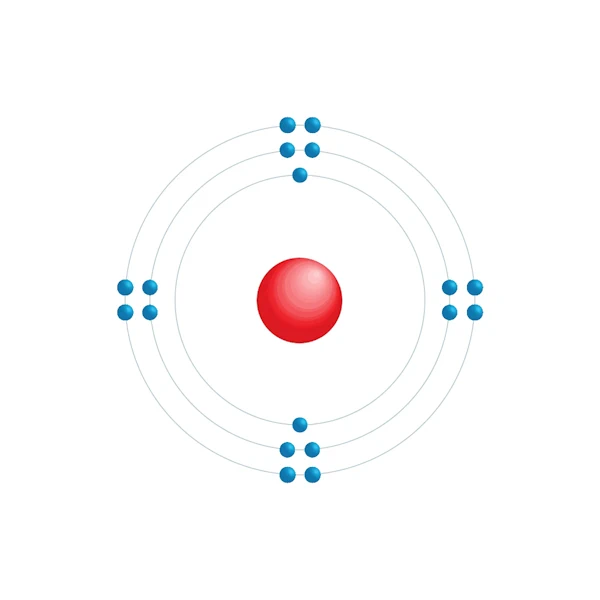
Elektroniskt konfigurationsschema
| Efternamn | Argon |
| Atomnummer | 18 |
| Atomisk massa | 39.948 |
| Symbol | Ar |
| Fusionspunkt | -189.4 |
| Kokpunkt | -185.9 |
| Densitet | 0.0017837 |
| Period | 3 |
| Grupp | 18 |
| Upptäckt | 1894 Rayleigh and Ramsay |
| Överflöd | 3.5 |
| Radie | 0.88 |
| Elektronnegativitet | 0 |
| Jonisering | 15.7596 |
| Isotopnummer | 8 |
| Elektronisk konfiguration | [Ne] 3s2 3p6 |
| Oxidationstillstånd | 0 |
| Elektron efter energinivå | 2,8,8 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se