Lista av föremål
»
Aktinium
»
Antimon
»
Argon
»
Arsenik
»
Barium
»
Bohrium
»
Bor
»
Brom
»
Cerium
»
Cesium
»
Curium
»
Dubnium
»
Erbium
»
Europium
»
Fermium
»
Fluor
»
Fosfor
»
Francium
»
Gallium
»
Guld
»
Hafnium
»
Helium
»
Holmium
»
Indium
»
Iridium
»
Järn
»
Jod
»
Kadmium
»
Kalcium
»
Kalium
»
Kalium
»
Kisel
»
Klor
»
Kobolt
»
Kol
»
Koppar
»
Krom
»
Krypton
»
Kväve
»
Lantan
»
Leda
»
Litium
»
Lutecium
»
Mangan
»
Molybden
»
Natrium
»
Neodym
»
Neon
»
Nickel
»
Nihonium
»
Niob
»
Nobelium
»
Osmium
»
Pengar
»
Platina
»
Polonium
»
Radium
»
Radon
»
Renium
»
Rodium
»
Rubidium
»
Rutenium
»
Samarium
»
Selen
»
Skandium
»
Svavel
»
Syre
»
Tallium
»
Tantal
»
Tellur
»
Tenn
»
Tennesse
»
Terbium
»
Thorium
»
Thulium
»
Titan
»
Uran
»
Vanadin
»
Väte
»
Vismut
»
Volfram
»
Xenon
»
Yttrium
»
Zink
He - Helium - INGEN ÄDELGASMETALL
Helium är det näst lättaste kemiska grundämnet på grundämnenas periodiska skala, och det vanligaste i universum. Dess atomnummer är 2 och dess atommassa är 4 003 amu (Atomic Mass Units).
helium är ett inert grundämne, det vill säga det reagerar inte på de flesta andra kemiska grundämnen. Den kombineras inte med andra element och är stabil vid rumstemperatur och tryck, förutom vid extrema förhållanden. Den har ingen lukt eller smak och är genomskinlig för synligt ljus.
helium är mycket lätt och har en smältpunkt på -452,2°F (-268,9°C). Dess kokpunkt är den högsta av alla grundämnen, vid -452,1°F (-268,9°C). Den är också mycket oreaktiv och kombinerar inte med andra element, vilket gör den till en utmärkt värmeisolator och en inert gas för att skydda andra brandfarliga gaser.
helium används i många industrier, inklusive kylning, fyrsystem och medicin. Den används också för att fylla ballonger och varmluftsblandare. Den används också vid tillverkning av fiberoptik, för belysning och personlig säkerhet. Slutligen används den för att fylla avgaserna från förbränningsmotorer, för att minska koldioxidutsläppen.
helium är ett inert grundämne, det vill säga det reagerar inte på de flesta andra kemiska grundämnen. Den kombineras inte med andra element och är stabil vid rumstemperatur och tryck, förutom vid extrema förhållanden. Den har ingen lukt eller smak och är genomskinlig för synligt ljus.
helium är mycket lätt och har en smältpunkt på -452,2°F (-268,9°C). Dess kokpunkt är den högsta av alla grundämnen, vid -452,1°F (-268,9°C). Den är också mycket oreaktiv och kombinerar inte med andra element, vilket gör den till en utmärkt värmeisolator och en inert gas för att skydda andra brandfarliga gaser.
helium används i många industrier, inklusive kylning, fyrsystem och medicin. Den används också för att fylla ballonger och varmluftsblandare. Den används också vid tillverkning av fiberoptik, för belysning och personlig säkerhet. Slutligen används den för att fylla avgaserna från förbränningsmotorer, för att minska koldioxidutsläppen.
Syntetisk
Radioaktiv
Flytande
Gasformig
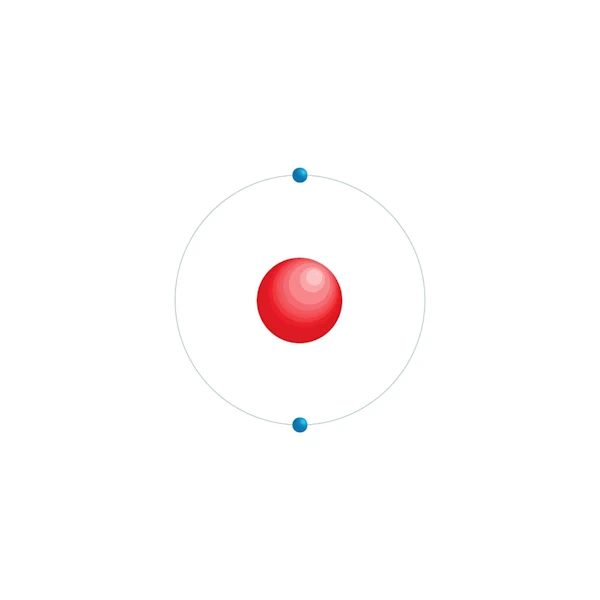
Elektroniskt konfigurationsschema
| Efternamn | Helium |
| Atomnummer | 2 |
| Atomisk massa | 4.002602 |
| Symbol | He |
| Fusionspunkt | -272.2 |
| Kokpunkt | -268.9 |
| Densitet | 0.0001785 |
| Period | 1 |
| Grupp | 18 |
| Upptäckt | 1868 Janssen |
| Överflöd | 0.008 |
| Radie | 0.49 |
| Elektronnegativitet | 0 |
| Jonisering | 24.5874 |
| Isotopnummer | 5 |
| Elektronisk konfiguration | 1s2 |
| Oxidationstillstånd | 0 |
| Elektron efter energinivå | 2 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se