Lista av föremål
»
Aktinium
»
Antimon
»
Argon
»
Arsenik
»
Barium
»
Bohrium
»
Bor
»
Brom
»
Cerium
»
Cesium
»
Curium
»
Dubnium
»
Erbium
»
Europium
»
Fermium
»
Fluor
»
Fosfor
»
Francium
»
Gallium
»
Guld
»
Hafnium
»
Helium
»
Holmium
»
Indium
»
Iridium
»
Järn
»
Jod
»
Kadmium
»
Kalcium
»
Kalium
»
Kalium
»
Kisel
»
Klor
»
Kobolt
»
Kol
»
Koppar
»
Krom
»
Krypton
»
Kväve
»
Lantan
»
Leda
»
Litium
»
Lutecium
»
Mangan
»
Molybden
»
Natrium
»
Neodym
»
Neon
»
Nickel
»
Nihonium
»
Niob
»
Nobelium
»
Osmium
»
Pengar
»
Platina
»
Polonium
»
Radium
»
Radon
»
Renium
»
Rodium
»
Rubidium
»
Rutenium
»
Samarium
»
Selen
»
Skandium
»
Svavel
»
Syre
»
Tallium
»
Tantal
»
Tellur
»
Tenn
»
Tennesse
»
Terbium
»
Thorium
»
Thulium
»
Titan
»
Uran
»
Vanadin
»
Väte
»
Vismut
»
Volfram
»
Xenon
»
Yttrium
»
Zink
I - Jod - HALOGEN SOM INTE ÄR METALL
Jod är ett metalloid kemiskt element som tillhör halogenfamiljen och som förekommer i fast form av en intensiv viol.
– jod är en extremt reaktiv halogen. Det kombineras med många andra kemiska element och bildar flyktiga molekyler.
– Den kombineras också med väte och bildar en flytande förening vid låga temperaturer som kallas jodvätesyra.
– Det är mycket lösligt i vatten och löser sig för att bilda jodidjoner.
– jod har många användningsområden, bland annat vid röntgen, rening av avloppsvatten för att avlägsna klor och bromider, och tillverkning av kemikalier, såsom antiseptika, läkemedel och färgämnen.
– Det används också vid behandling av vissa cancerformer och vid framställning av radiofarmaka för medicinska diagnostiska undersökningar.
– jod används också vid framställning av radioaktivt jod, som används i applikationer som radioavbildning och cancerbehandling.
– jod är en extremt reaktiv halogen. Det kombineras med många andra kemiska element och bildar flyktiga molekyler.
– Den kombineras också med väte och bildar en flytande förening vid låga temperaturer som kallas jodvätesyra.
– Det är mycket lösligt i vatten och löser sig för att bilda jodidjoner.
– jod har många användningsområden, bland annat vid röntgen, rening av avloppsvatten för att avlägsna klor och bromider, och tillverkning av kemikalier, såsom antiseptika, läkemedel och färgämnen.
– Det används också vid behandling av vissa cancerformer och vid framställning av radiofarmaka för medicinska diagnostiska undersökningar.
– jod används också vid framställning av radioaktivt jod, som används i applikationer som radioavbildning och cancerbehandling.
Syntetisk
Radioaktiv
Flytande
Gasformig
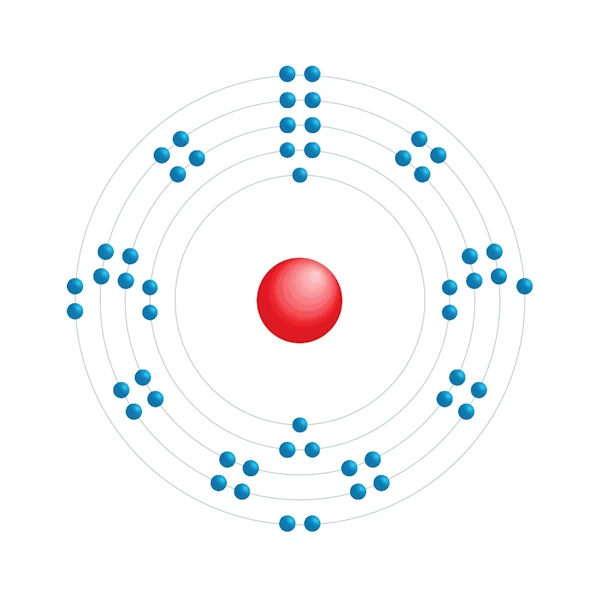
Elektroniskt konfigurationsschema
| Efternamn | Jod |
| Atomnummer | 53 |
| Atomisk massa | 126.90447 |
| Symbol | I |
| Fusionspunkt | 113.5 |
| Kokpunkt | 184.4 |
| Densitet | 4.93 |
| Period | 5 |
| Grupp | 17 |
| Upptäckt | 1811 Courtois |
| Överflöd | 0.45 |
| Radie | 1.3 |
| Elektronnegativitet | 2.66 |
| Jonisering | 10.4513 |
| Isotopnummer | 24 |
| Elektronisk konfiguration | [Kr] 4d10 5s2 5p5 |
| Oxidationstillstånd | -1,1,3,5,7 |
| Elektron efter energinivå | 2,8,18,18,7 |
| Mineral- | Hårdhet | Densitet |
| Aurivilliusite | 8.96 | |
| Bellingerite | 4.00 / 4.00 | 4.89 |
| Bluebellite | 1.00 / 1.00 | 4.75 |
| Brüggenite | 3.50 / 3.50 | 4.24 |
| Capgaronnite | 6.19 | |
| Carlosruizite | 2.50 / 3.00 | 3.42 |
| Coccinite | 2.00 / 2.00 | 6.00 |
| Demicheleite-(Br) | ||
| Demicheleite-(I) | ||
| Dietzeite | 3.50 / 3.50 | 3.62 |
| Fuenzalidaite | 2.50 / 3.00 | 3.31 |
| George-ericksenite | 3.00 / 4.00 | 3.04 |
| Grechishchevite | 2.50 / 2.50 | 7.16 |
| Hectorfloresite | 2.00 / 2.00 | 2.80 |
| Iodargyrite | 1.50 / 2.00 | 5.50 |
| Iodine | ||
| Lautarite | 3.50 / 4.00 | 4.52 |
| Marshite | 2.50 / 2.50 | 5.60 |
| Miersite | 2.50 / 3.00 | 5.64 |
| Moschelite | 1.50 / 2.00 | 7.00 |
| Mutnovskite | 2.00 / 2.00 | 6.18 |
| Nataliyamalikite | ||
| Perroudite | 2.00 / 2.00 | |
| Radtkeite | 2.00 / 3.00 | 7.00 |
| Salesite | 3.00 / 3.00 | 4.77 |
| Schwartzembergite | 2.50 / 2.50 | 7.39 |
| Seeligerite | 6.83 | |
| Tedhadleyite | 2.50 / 2.50 | |
| Tocornalite | 1.00 / 2.00 | |
| Vasilyevite | 3.00 / 3.00 | 9.57 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se