Lista av föremål
»
Aktinium
»
Antimon
»
Argon
»
Arsenik
»
Barium
»
Bohrium
»
Bor
»
Brom
»
Cerium
»
Cesium
»
Curium
»
Dubnium
»
Erbium
»
Europium
»
Fermium
»
Fluor
»
Fosfor
»
Francium
»
Gallium
»
Guld
»
Hafnium
»
Helium
»
Holmium
»
Indium
»
Iridium
»
Järn
»
Jod
»
Kadmium
»
Kalcium
»
Kalium
»
Kalium
»
Kisel
»
Klor
»
Kobolt
»
Kol
»
Koppar
»
Krom
»
Krypton
»
Kväve
»
Lantan
»
Leda
»
Litium
»
Lutecium
»
Mangan
»
Molybden
»
Natrium
»
Neodym
»
Neon
»
Nickel
»
Nihonium
»
Niob
»
Nobelium
»
Osmium
»
Pengar
»
Platina
»
Polonium
»
Radium
»
Radon
»
Renium
»
Rodium
»
Rubidium
»
Rutenium
»
Samarium
»
Selen
»
Skandium
»
Svavel
»
Syre
»
Tallium
»
Tantal
»
Tellur
»
Tenn
»
Tennesse
»
Terbium
»
Thorium
»
Thulium
»
Titan
»
Uran
»
Vanadin
»
Väte
»
Vismut
»
Volfram
»
Xenon
»
Yttrium
»
Zink
Cs - Cesium - ALKALIMETALL
Cesium är en grupp 1-metall i det periodiska systemet. Dess kemiska grundämne är Cs och den har ett atomnummer på 55. Dess atommassa är 132,905 g/mol och dess smältpunkt är 28°C, vilket gör den mycket formbar och ger den en mycket låg densitet. Den har en silverfärg och lyser i mörkret, vilket ger den smeknamnet "blank metall".
cesium har mycket höga reaktiva egenskaper. Den reagerar mycket lätt med syre och vatten och kan till och med reagera med koppar vid rumstemperatur. Det används i mycket stor utsträckning inom industrin som katalysator i kemiska processer, särskilt under produktionen av petroleumprodukter.
Ur medicinsk synvinkel används cesium för att behandla olika sjukdomar, inklusive cancer och Parkinsons sjukdom. Det används också som baskemikalie vid tillverkning av läkemedel och farmaceutiska föreningar.
cesium används också inom elektronikindustrin på grund av dess ledande egenskaper och dess förmåga att producera alfapartiklar. Det används ofta vid tillverkning av dioder, transistorer och integrerade kretsar.
cesium används också i halogenlampor och konstverk, där det används för sina exceptionella termiska och galvaniska egenskaper. Metallurgi och flygindustrin använder också cesium för dess mekaniska och elektrokemiska egenskaper.
cesium har mycket höga reaktiva egenskaper. Den reagerar mycket lätt med syre och vatten och kan till och med reagera med koppar vid rumstemperatur. Det används i mycket stor utsträckning inom industrin som katalysator i kemiska processer, särskilt under produktionen av petroleumprodukter.
Ur medicinsk synvinkel används cesium för att behandla olika sjukdomar, inklusive cancer och Parkinsons sjukdom. Det används också som baskemikalie vid tillverkning av läkemedel och farmaceutiska föreningar.
cesium används också inom elektronikindustrin på grund av dess ledande egenskaper och dess förmåga att producera alfapartiklar. Det används ofta vid tillverkning av dioder, transistorer och integrerade kretsar.
cesium används också i halogenlampor och konstverk, där det används för sina exceptionella termiska och galvaniska egenskaper. Metallurgi och flygindustrin använder också cesium för dess mekaniska och elektrokemiska egenskaper.
Syntetisk
Radioaktiv
Flytande
Gasformig
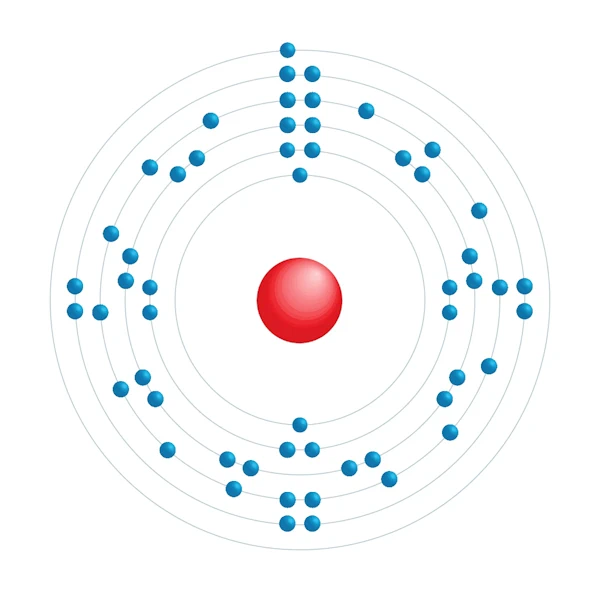
Elektroniskt konfigurationsschema
| Efternamn | Cesium |
| Atomnummer | 55 |
| Atomisk massa | 132.90545196 |
| Symbol | Cs |
| Fusionspunkt | 28.4 |
| Kokpunkt | 690 |
| Densitet | 1.873 |
| Period | 6 |
| Grupp | 1 |
| Upptäckt | 1860 Bunsen and Kirchoff |
| Överflöd | 3 |
| Radie | 3.3 |
| Elektronnegativitet | 0.79 |
| Jonisering | 3.8939 |
| Isotopnummer | 22 |
| Elektronisk konfiguration | [Xe] 6s1 |
| Oxidationstillstånd | 1 |
| Elektron efter energinivå | 2,8,18,18,8,1 |
| Mineral- | Hårdhet | Densitet |
| Avogadrite | 2.62 | |
| Caesiumpharmacosiderite | ||
| Cesiodymite | ||
| Cesplumtantite | 7.00 / 7.00 | 6.00 |
| Dachiardite-Ca | 4.00 / 4.50 | 2.14 |
| Gainesite | 4.00 / 4.00 | 2.94 |
| Galkhaite | 3.00 / 3.00 | 5.40 |
| Kirchhoffite | 6.00 / 6.50 | 3.64 |
| Kupletskite-(Cs) | 4.00 / 4.00 | 3.68 |
| Londonite | 8.00 / 8.00 | 3.34 |
| Margaritasite | 2.00 / 2.00 | 5.40 |
| Mccrillisite | 4.50 / 4.50 | 3.12 |
| Mendeleevite-(Ce) | ||
| Mendeleevite-(Nd) | 5.00 / 5.50 | 3.16 |
| Nalivkinite | 3.29 | |
| Nanpingite | 2.50 / 3.00 | 3.11 |
| Natrobistantite | 6.10 | |
| Odigitriaite | 5.00 / 5.00 | 2.83 |
| Pautovite | 2.50 / 2.50 | 3.85 |
| Pezzottaite | 8.00 / 8.00 | 2.97 |
| Pollucite | 6.50 / 6.50 | 2.90 |
| Potassicmendeleevite-(Ce) | ||
| Ramanite-(Cs) | ||
| Rhodizite | 8.50 / 8.50 | 3.44 |
| Senkevichite | 5.50 / 6.00 | 3.13 |
| Sokolovaite | ||
| Telyushenkoite | 6.00 / 6.00 | 2.73 |
| Zeravshanite | 6.00 / 6.00 | 3.09 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se