Lista av föremål
»
Aktinium
»
Antimon
»
Argon
»
Arsenik
»
Barium
»
Bohrium
»
Bor
»
Brom
»
Cerium
»
Cesium
»
Curium
»
Dubnium
»
Erbium
»
Europium
»
Fermium
»
Fluor
»
Fosfor
»
Francium
»
Gallium
»
Guld
»
Hafnium
»
Helium
»
Holmium
»
Indium
»
Iridium
»
Järn
»
Jod
»
Kadmium
»
Kalcium
»
Kalium
»
Kalium
»
Kisel
»
Klor
»
Kobolt
»
Kol
»
Koppar
»
Krom
»
Krypton
»
Kväve
»
Lantan
»
Leda
»
Litium
»
Lutecium
»
Mangan
»
Molybden
»
Natrium
»
Neodym
»
Neon
»
Nickel
»
Nihonium
»
Niob
»
Nobelium
»
Osmium
»
Pengar
»
Platina
»
Polonium
»
Radium
»
Radon
»
Renium
»
Rodium
»
Rubidium
»
Rutenium
»
Samarium
»
Selen
»
Skandium
»
Svavel
»
Syre
»
Tallium
»
Tantal
»
Tellur
»
Tenn
»
Tennesse
»
Terbium
»
Thorium
»
Thulium
»
Titan
»
Uran
»
Vanadin
»
Väte
»
Vismut
»
Volfram
»
Xenon
»
Yttrium
»
Zink
mineralogi
element
Ga Gallium
Ga - Gallium - DÅLIG METALL
Gallium är ett metalliskt kemiskt grundämne med symbolen Ga. Det är det kemiska grundämnet med atomnummer 31 och atommassa 69,723 g/mol. Dess atomära bindningsenergi är 624,5 kJ/mol.
gallium har en monoatomisk atom som gör kovalenta bindningar med andra atomer. Den har en kubisk struktur med mittytor. Dess färg är silvergrå och den har en relativt låg hårdhet.
gallium har en mycket låg smälttemperatur (29,76°C) och en koktemperatur (2402°C). Dess smältpunkt används för generella sensorer eftersom den reagerar med värme och ger exakt temperaturkontroll.
gallium är mycket lösligt i organiska material och i starka syror, men det är olösligt i vatten. Det blandas också lätt med andra element för att bilda legeringar.
gallium används även vid tillverkning av lysdioder (solid-state lighting) och inom datorindustrin för tillverkning av processorer, minne och integrerade kretsar.
gallium används också inom den medicinska industrin för produktion av radiofarmaka och diagnostiska produkter. Det används också vid tillverkning av kosmetika och läkemedel. Det används också inom materialindustrin på grund av dess termiska och kemiska egenskaper.
gallium har en monoatomisk atom som gör kovalenta bindningar med andra atomer. Den har en kubisk struktur med mittytor. Dess färg är silvergrå och den har en relativt låg hårdhet.
gallium har en mycket låg smälttemperatur (29,76°C) och en koktemperatur (2402°C). Dess smältpunkt används för generella sensorer eftersom den reagerar med värme och ger exakt temperaturkontroll.
gallium är mycket lösligt i organiska material och i starka syror, men det är olösligt i vatten. Det blandas också lätt med andra element för att bilda legeringar.
gallium används även vid tillverkning av lysdioder (solid-state lighting) och inom datorindustrin för tillverkning av processorer, minne och integrerade kretsar.
gallium används också inom den medicinska industrin för produktion av radiofarmaka och diagnostiska produkter. Det används också vid tillverkning av kosmetika och läkemedel. Det används också inom materialindustrin på grund av dess termiska och kemiska egenskaper.
Syntetisk
Radioaktiv
Flytande
Gasformig
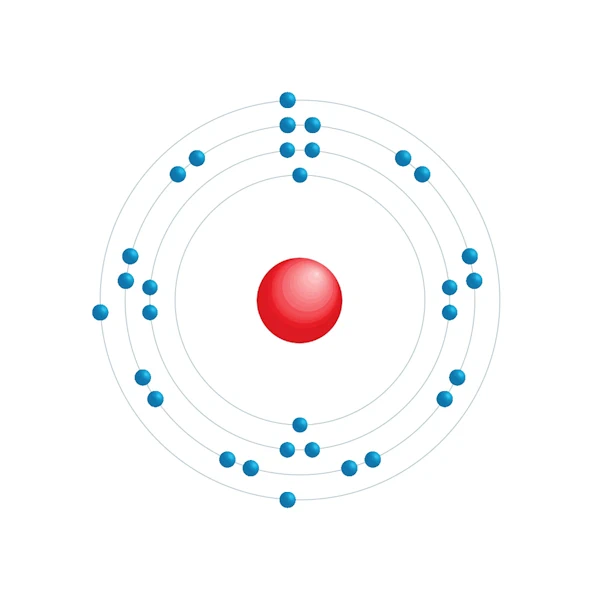
Elektroniskt konfigurationsschema
| Efternamn | Gallium |
| Atomnummer | 31 |
| Atomisk massa | 69.723 |
| Symbol | Ga |
| Fusionspunkt | 29.8 |
| Kokpunkt | 2403 |
| Densitet | 5.907 |
| Period | 4 |
| Grupp | 13 |
| Upptäckt | 1875 de Boisbaudran |
| Överflöd | 19 |
| Radie | 1.8 |
| Elektronnegativitet | 1.81 |
| Jonisering | 5.9993 |
| Isotopnummer | 14 |
| Elektronisk konfiguration | [Ar] 3d10 4s2 4p1 |
| Oxidationstillstånd | 1,2,3 |
| Elektron efter energinivå | 2,8,18,3 |
| Mineral- | Hårdhet | Densitet |
| Calvertite | 4.00 / 5.00 | 5.24 |
| Dissakisite-(La) | 6.50 / 7.00 | 3.79 |
| Eyselite | 3.64 | |
| Ferrohögbomite-2N2S | 6.00 / 7.00 | |
| Gallite | 3.00 / 3.50 | 4.20 |
| Gallobeudantite | 4.00 / 4.00 | 4.58 |
| Galloplumbogummite | 4.62 | |
| Ishiharaite | ||
| Krieselite | 5.50 / 6.50 | 4.07 |
| Maikainite | 4.00 / 4.00 | 4.45 |
| Ovamboite | 3.50 / 3.50 | 4.74 |
| Söhngeite | 4.00 / 4.50 | 3.84 |
| Tsumgallite | 1.50 / 2.50 | 5.08 |
| Zincobriartite |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se